近日,齐鲁工业大学材料学部氢电能源材料创新团队在《Composites Part B》上报道了一种二维层状金属有机框架材料SUM-1(Zr)的优异气体分离性能。通过利用材料中电负性氧原子作为氢键供体,能够高效捕获乙炔分子,并借助乙炔与二氧化碳分子之间的竞争吸附机制,实现了乙炔/二氧化碳混合气体的高效分离,展示了MOFs材料在混合气体分离领域的巨大潜力。材料学部联合培养博士研究生谢文鹏是该论文的第一作者,材料学部讲师付秋菊博士、南昆士兰大学Lei Ge教授、齐鲁工大赵学波教授为论文的联合通讯作者。Composites Part B是中科院一区Top期刊,影响因子12.7,是国际材料领域的重要期刊,具有很大的国际学术影响力。

乙炔是工业有机化学领域的重要基础原料,广泛应用于合成多种化学产品,例如丙烯腈、醋酸以及合成纤维。工业上,乙炔的生产主要通过甲烷的部分燃烧或烃类的热裂解实现。然而,在此过程中通常会生成二氧化碳等杂质,这些杂质可能对后续应用产生不利影响,因此在实际应用之前必须对其进行提纯。然而,由于乙炔和二氧化碳具有相似的尺寸大小,这一分离过程面临显著的技术挑战。目前,溶剂萃取工艺和低温蒸馏技术是分离乙炔/二氧化碳混合气体的主要方法,但这些传统技术往往能耗较高,并对环境造成了一定的影响。相比之下,基于物理吸附机制的吸附分离方法提供了一种更为节能且环境友好的替代方案。
利用多孔固体材料进行吸附分离被广泛认为是一种前景广阔的技术,能够有效替代传统方法并显著降低能耗。金属有机框架(MOFs)由无机结构单元与有机配体通过自组装形成,因其在气体存储和分离领域的优异性能而备受关注。一般来说,具有较大孔径的MOFs材料可以加速吸附质分子的扩散过程,从而大幅缩短达到吸附平衡所需的时间;而较小孔径的MOFs材料由于与目标分子之间存在更强的作用力,虽然能够实现更高的选择性,但吸附质分子达到动力学平衡的时间相对较长。鉴于乙炔和二氧化碳在四极矩及静电势方面的显著差异,通过乙炔与强氢键供体之间的相互作用,可以在乙炔/二氧化碳混合气体分离过程中实现对乙炔分子的高效捕获。
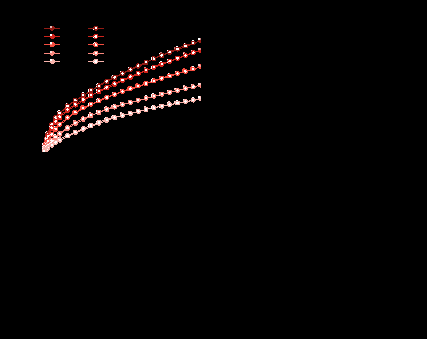
图1 SUM-1(Zr)在268 K、273 K、283 K、298 K和313 K温度下对(a)乙炔和(b)二氧化碳的单组分吸附等温线;在650 mbar和 298 K条件下(c)乙炔和(d)二氧化碳在SUM-1(Zr)上的吸附动力学曲线(以点表示)及拟合曲线(以线表示)。
SUM-1(Zr)在沿晶体学z轴方向呈现出一个孔径约为1.60 nm的一维六边形通道,以及一个孔径约为0.63 nm的三角形通道。在x轴方向上,其平面结构由二维层状排列构成,层间距约为0.45 nm。在298 K和1 bar条件下,SUM-1(Zr)对乙炔的吸附量为3.07 mmol g-1,对二氧化碳的吸附量为1.72 mmol g-1。鉴于SUM-1(Zr)的孔径远大于乙炔和二氧化碳的动力学直径,这两种气体在其孔隙内的扩散阻力较小,较大的动力学常数(k₁)对应于吸附质分子沿晶体学z轴方向的六边形通道的扩散,而较小的动力学常数(k₂)则对应于沿同一方向的三角形通道的扩散,具有较大孔径的六边形通道在促进乙炔和二氧化碳的快速扩散方面起着关键作用。
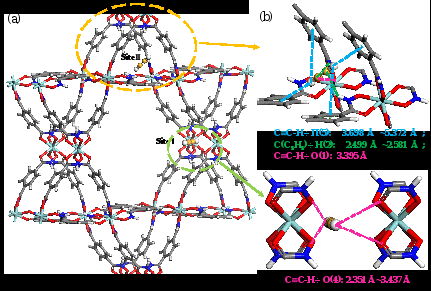
图2(a)乙炔在SUM-1(Zr)两个孔道内的优先吸附结合位点;(b)乙炔在SUM-1(Zr)三角形孔道内的优先吸附位点;(c)乙炔在SUM-1(Zr)六边形孔道内的优先吸附位点。
GCMC和DFT理论计算表明,乙炔分子优先吸附在SUM-1(Zr)六边形通道中的氧原子附近(位点Ⅰ),并通过与来自相邻平行层的H2BDHA的四个氧原子形成四个C≡C-H…O氢键(键长范围为2.351至 3.437 Å),其结合能为50.8555 kJ/mol。在三角形通道中,乙炔分子更倾向于吸附在H2BDHA配体的苯环附近(位点II)。在此位点,乙炔分子与H2BDHA配体的一个氧原子形成一个 C≡C-H…O氢键(键长为3.395 Å),同时与来自相邻平行层的苯环和氨基基团之间形成了多重范德华相互作用(距离范围为2.499 Å至5.372 Å),其结合能为 47.0588 kJ/mol。在两种不同孔道中,SUM-1(Zr)对乙炔的结合能均高于对二氧化碳的结合能,这表明乙炔和二氧化碳之间存在竞争吸附行为。
本研究提出了一种基于电负性氧原子作为氢键供体的新型分离机制,并进一步揭示了通过较大孔径和利用吸附质分子间的竞争吸附效应来提升混合气体分离性能及动力学扩散速率的重要潜力。
原文链接:https://www.sciencedirect.com/science/article/pii/S1359836825003063





